Quina diferència hi ha entre les piles alcalines i les de sal?
Molt sovint a les prestatgeries de les botigues hi ha bateries barates una al costat de l'altra que semblen ser exactament les mateixes, però molt més cares. Amb què està connectat això? El cas és que les piles poden ser salines o alcalines. Intentem esbrinar com són semblants i en què es diferencien, excepte pel preu.
El contingut de l'article
Bateries de sal
El primer prototip va aparèixer gràcies al "vol del pensament" de l'inventor italià Alessandro Volta l'any 1800. Aquest va ser el prototip de la moderna bateria de sal. Simplement va agafar i combinar diversos discos de zinc i plata amb cartró en un, que va remullar amb una solució de sal. I només llavors els científics de tot el món van millorar aquesta tecnologia i l'aparença del dispositiu.
Vint anys més tard, el científic britànic John Daniel va presentar un producte que utilitzava zinc i sulfat de coure com a electròlit. La potència d'aquest producte era d'1,1 volts, però, si s'utilitza en dispositius que no requereixen molta electricitat, la seva càrrega seria suficient per a cent anys de funcionament.
Característiques de composició i disseny
Durant molt de temps, aquesta bateria va estar per davant d'altres de demanda, això no es va impedir ni tan sols pel fet que les bateries pràcticament no han canviat des de la seva creació, ni externament ni internament.Combinant perfectament característiques d'alta qualitat i preus econòmics, van liderar amb confiança les vendes.
L'interior és molt senzill. La base de la bateria és l'ànode, que es presenta en forma de zinc en pols. La part activa de la bateria està impregnada de diòxid de manganès. Al càtode fet de zinc es van afegir elements anticorrosius i, naturalment, un electròlit, el paper del qual juga el clorur d'amoni. De fet, va ser el clorur d'amoni el que va donar nom a la bateria, ja que l'electròlit que hi ha no és més que sal.
Els elèctrodes de la cèl·lula estan separats per separadors; separen el reactiu, evitant que entri en contacte, però al mateix temps no impedeixen la penetració de l'electròlit. Com a resultat, comença a produir-se una reacció a l'interior, que és la causa de l'aparició del corrent elèctric. Flueix als elements nutritius instal·lats a l'interior, i a través d'ells als elèctrodes, continuant el seu moviment fins a l'aparell on es col·loca la bateria.
Tipus i dimensions
Al món de l'electrònica hi ha un gran nombre de diferents tipus de bateries de sal. Tots aquests tipus i mides han adquirit des de fa temps la seva pròpia designació. El cas és que es va decidir que seria molt més fàcil distingir-los si estiguessin marcats amb lletres i números. Aquesta solució va néixer a les entranyes de la Comissió Electrotècnica Internacional, però a més, hi ha classificacions similars disponibles al nostre GOST, TU, així com a la ANSI/NEDA importada.
Fa temps que estem acostumats a dos tipus de bateries, que són fàcilment diferents fins i tot en aparença. Aquestes són les bateries dels dits i els petits. D'acord amb la classificació, se'ls assignen les denominacions AA i AAA, respectivament. Tots dos tenen una tensió d'1,5 volts.La forma de les bateries sembla un cilindre allargat.
Però a més d'aquestes dues, hi ha tres varietats més a les botigues. És molt habitual veure piles classificades com a C o LR 14. Sembla un petit barril.
Les bateries més grans (també en forma de barril, però més grans) es van produir una vegada específicament per a llanternes. Portaven la marca D o LR 20, però a més d'utilitzar-se en llanternes, encaixaven perfectament en les gravadores.
Durant la Unió Soviètica, es va llançar la producció de bateries R10. Van trobar la seva aplicació en diversos instruments de mesura i... en joguines.
Si observeu bé les bateries cilíndriques, notareu una protuberància en un extrem; el plus de les bateries es troba en aquest lloc. No hi ha ressalts a l'altre extrem, i com que no n'hi ha, això significa que és un menys. I en una bateria de forma rectangular 6 F22, o com es diu popularment, corona, hi ha dos ressalts a la part superior. Tant el més com el menys es col·loquen en un sol lloc.
Avantatges i inconvenients
Si parlem del bo i del dolent, hem d'admetre que els avantatges de les piles de sal són la lleugeresa i el baix cost. Aquestes són les seves principals cartes de triomf. Si no els exploteu sense pietat, i de vegades els doneu un descans, aleshores duraran una mica més. Fins i tot si s'asseuen, es poden reviure breument sacsejant-los a fons o colpejant-los amb la mà. Amb aquestes accions impactants forçarem l'electròlit arrugat a aplanar-se.
Però hi haurà una mica més de "trist" en aquestes piles:
- no duren prou (tres anys i no més);
- encara que no s'utilitzi la bateria, es descarregarà;
- l'electròlit tendeix a assecar-se amb el temps;
- en condicions de canvis de temperatura freqüents, la bateria funciona molt inestable;
- Aquesta bateria té alguns problemes relacionats amb l'estanquitat, per tant és possible que hi hagi tot tipus de fuites. Com a regla general, això passa si la bateria no s'utilitza durant molt de temps; això fa que la carcassa s'oxidi, cosa que inevitablement causarà danys a l'equip on està instal·lat;
- i el principal desavantatge és el baix consum d'energia.
Piles alcalines
Les piles alcalines van aparèixer més tard. Només a principis del segle XX van ser desenvolupats pels nord-americans Waldemar Jungner i Thomas Edison, però van trigar molt a fer-se populars. S'anomenen alcalines perquè així sona la paraula "àlcali" en anglès.
Característiques de disseny
Com que les piles alcalines es van inventar més tard que les de sal, es van posar a la venda més tard. La primera empresa que va llançar la seva producció va ser Duracell, coneguda per molts. Encara manté una posició de lideratge en aquest àmbit. Només recordeu el seu conill amb una bateria. Aquesta bateria de "conill" en particular pertany a la família alcalina.
La base d'aquesta bateria, com en el cas d'una bateria de sal, és l'ànode, que té la forma d'una massa en pols, que està impregnada d'electròlit. Aquesta cèl·lula galvànica utilitza diòxid de manganès, que actua com a càtode. L'electròlit de la bateria és àlcali.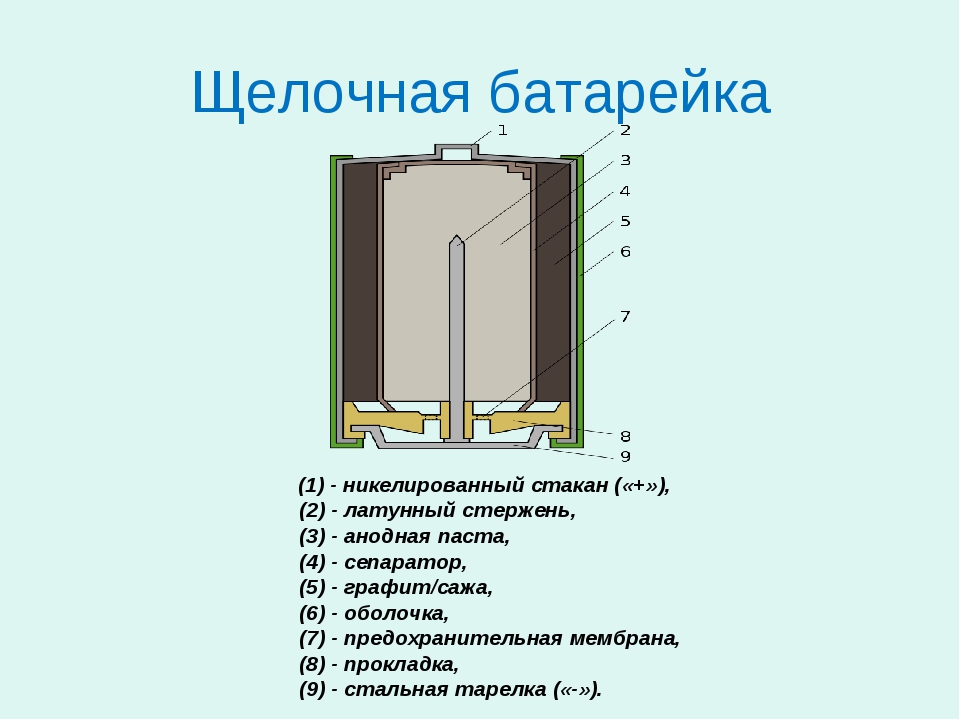
Fonamentalment, el funcionament d'una bateria alcalina no és diferent d'una bateria de sal, però la seva producció és més alta. Un agent reductor fet de zinc redueix el risc que el metall perdi la seva activitat si es produeix una forta descàrrega de corrent. A més, l'elèctrode de zinc en pols permet augmentar el percentatge de substància activa en comparació amb les bateries de sal. I gràcies a l'electròlit utilitzat: àlcali, la capacitat augmenta, que és deu vegades més gran que la dels anàlegs de sal.
Avantatges i inconvenients
Trets positius:
- alta intensitat energètica;
- mostra excel·lents resultats de rendiment a càrregues mitjanes;
- autodescàrrega molt lenta;
- no perd rendiment a baixes temperatures;
- ben segellat;
- té un llarg període de funcionament: de set a deu anys.
Qualitats negatives:
- pes considerable;
- preu alt;
- Si l'electròlit es descarrega, la bateria es torna immediatament inutilitzable.
Què distingeix les piles alcalines de les de sal?
Les piles de sal més habituals són les de zinc. La sal es va utilitzar com a electròlit en aquesta cel·la galvànica.
Referència. Pel que fa a l'eficiència operativa, les bateries alcalines estan set vegades per davant dels "competidors".
A les piles alcalines, la sal com a electròlit es va substituir per àlcali. Això va fer que el seu rendiment fos millor que el seu homòleg de sal. Durant la producció, van abandonar el cos de zinc i van decidir utilitzar el mateix metall, però en forma de pols. Per tant, quan l'àlcali va interactuar amb l'ànode i el càtode, es va començar a alliberar molta més energia.
Les bateries de sal a base de zinc són capaços de funcionar en un rang de temperatures des de menys vint fins a més setanta graus. Es poden utilitzar en una gran varietat de dispositius. La vida operativa és de dos o tres anys.
Referència. De mitjana, la potència d'una bateria de sal és d'un volt i mig.
Les piles alcalines tenen una vida útil més llarga. La seva conservació sense pèrdua de propietats beneficioses arriba als deu anys.L'ús d'àlcali com a electròlit els permet mantenir les seves propietats de treball fins i tot a baixes temperatures. Les seves dimensions coincideixen amb les piles de sal.
Fins fa poc, les fonts d'alimentació alcalines no tenien la capacitat de recarregar-se, però les darreres novetats han permès obtenir-la. Ara es poden utilitzar repetidament i poden mantenir la seva càrrega durant molt de temps. Això els va fer més respectuosos amb el medi ambient i els va donar un avantatge afegit.
Aquesta bateria satisfà les necessitats creixents del mercat, les demandes d'energia del qual creixen constantment.
Com distingir-los
Si desmunteu una pila de sal i una pila alcalina, les diferències entre elles de seguida us cridaran l'atenció, però qui us permetrà fer-ho en una botiga? Però, llavors, com no es pot equivocar en triar si exteriorment no són diferents?
Hi ha una sortida. En primer lloc, la diferència serà el cost de la bateria. Com que les piles alcalines són més cares de produir, costen molt més. A més, al cos de la pila alcalina hi ha la inscripció ALKALINE, que en traducció significa àlcali.





